[KHDH] [Môn Hóa học] Hợp chất của cacbon
27/12/2020
Tiết 26- Bài 16. HỢP CHẤT CỦA CACBON (Tiết 1)
I. Mục tiêu1. Kiến thức
* HS nêu được:
- Tính chất vật lí của CO, CO2.
- Số oxi hóa của C trong hợp chất
- Tính chất hóa học của khí CO,CO2.
- Ứng dụng, cách điều chế CO,CO2.
* HS giải thích được:
- Vai trò của khí CO đối với sản xuất công nghiệp, vai trò của khí CO2 đối với động vật, thực vật và đời sống con người.
- Tác hại của khí CO đối với con người.
* HS vận dụng được:
- Biết cách phòng chống và sơ cứu ngộ độc khí than.
- Biết cách dập các đám cháy thông thường, biết phương pháp chế biến nước giải khát có gas và cách sử dụng hợp lí.
- Có ý thức bảo vệ môi trường.
2. Kĩ năng
- Tìm hiểu, thu thập thông tin, xử lý thông tin để rút ra kết luận.
- Tiến hành một số thí nghiệm cơ bản
3. Thái độ
- Nhận thức rõ vai trò của khí CO,CO2 đối với động vật và thực vật, tác hại của khí CO,CO2 đối với môi trường.
- Có ý thức phòng chống ngộ độc khí than cho cơ thể và giảm tác hại của khí CO đối với môi trường.
- Có ý thức bảo vệ môi trường để hành tinh của chúng ta mãi xanh.
4. Những năng lực chủ yếu cần hướng tới
- Năng lực hợp tác.
- Năng lực thực hành
- Năng lực sử dụng ngôn ngữ hóa học
- Năng lực giải quyết vấn đề và sáng tạo thông qua môn hóa học.
- Năng lực tự học.
II. Chuẩn bị củaGV và HS
1.Giáo viên
- Kế hoạch dạy học
- Slide dạy học
- Dụng cụ, hóa chất: Đá khô, NaOH, nước vôi trong, nước cất, nến, phenolphtalein, bình tam giác, cốc thủy tinh, bóng bay, vỏ chai nước.
- Phiếu học tập cho học sinh
2.Học sinh:
- Chuẩn bị bài theo các câu hỏi định hướng của tiết trước: (C có thể tạo những oxit nào, tính chất vật lý, hóa học và điều chế ra sao, chúng có ứng dụng gì ảnh hưởng như thế nào đến đời sống và môi trường)
- Kê bàn ghế theo nhóm và phân công nhóm trưởng
III. Chuỗi các hoạt động học
1. Hoạt động khởi động (5 phút) : Trò chơi tảng băng trôi
Mục tiêu hoạt động
- Tạo hứng thú cho giờ học
- Hướng học sinh vào nội dung chính của bài nghiên cứu các oxit của Cacbon trong đó CO2 là nguyên nhân chính gây hiệu ứng nhà kính làm trái đất nóng lên → băng tan (phù hợp tên trò chơi)
Phương thức tổ chức hoạt động
- GV hướng dẫn trò chơi: “Để khởi động cho tiết học ngày hôm nay, cô và cả lớp sễ tham gia trò chơi có tên: Tảng băng trôi. Trái đất nóng lên khiến băng tan ra, chim cánh cụt con bị tách khỏi bố mẹ, bằng cách trả lời các câu hỏi liên quan đến kiến thức hóa học, các em có thể kéo các tảng băng khác lại gần để đưa chim cánh cụt con về nhà.”
- 3 HS lần lượt trả lời các câu hỏi:
+ Khi đốt cacbon trong không khí, sản phẩm thu được ngoài khí ……… còn có một ít khí …….. (CO2, CO)
+ Số oxi hóa của cacbon trong CO và CO2 lần lượt là …………(+2,+4)
+ Dựa vào tính chất hóa học, người ta chia oxit thành 4 loại: oxit axit, oxit bazơ, oxit lưỡng tính và ………. (Oxit trung tính – Oxit không tạo muối)
- GV đặt vấn đề: “Như vậy bằng kiến thức hóa học của mình các em đã cứu được chim cánh cụt con, khi học hóa các em sẽ có biện pháp làm chậm lại hiện tượng băng tan ra ở các cực đấy. Các em có biết vì sao băng tan không? (Hs: Hiệu ứng nhà kính/Trái đất nóng lên) CO2 – một oxit của Cacbon là nguyên nhân chính gây hiệu ứng nhà kính. Cacbon có 2 oxit là CO, CO2, chúng có những tính chất gì và ảnh hưởng như thế nào đến đời sống mời các em cùng tìm hiểu nội dung bài học ngày hôm nay : Bài 16: Hợp chất Cacbon (Tiết 1)”
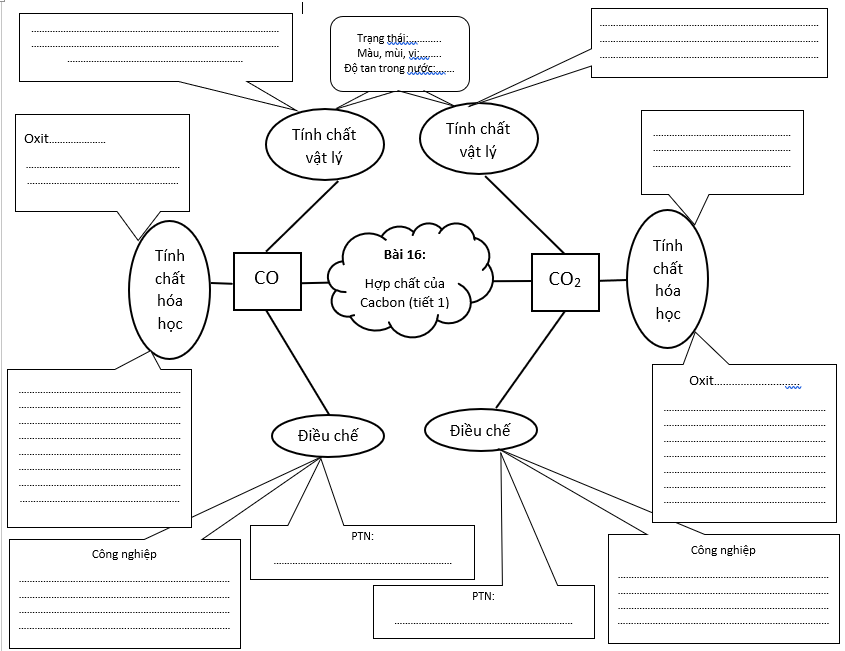
- GV cung cấp sơ đồ tư duy (chưa hoàn thiện) của bài, yêu cầu học sinh hoàn thiện dần qua các nội dung bài học. Thông báo vào cuối tiết, giáo viên sẽ thu một số sản phẩm sơ đồ tư duy để đánh giá khả năng tiếp nhận kiến thức của học sinh. (Lưu ý: Phần trình bày bảng của giáo viên tương tự sơ đồ tư duy của học sinh để học sinh dễ theo dõi và cuối bài học sinh có thể nhìn vào sơ đồ tư duy để tổng kết nội dung bài học)
Hoạt động 1. Tìm hiểu tính chất vật lý của khí CO ( 3 phút)
Mục tiêu hoạt động
Nêu được tính chất vật lý CO, đặc biệt tính độc, biết cách phòng tránh ngộ độc CO
Phương thức tổ chức hoạt động
- GV: Các em hãy dựa vào sgk và các kiến thức thực tiễn cho cô biết các tính chất vật lý của khí CO
- Hs : + CO là chất khí
+ Không màu không mùi, không vị
+ Hơi nhẹ hơn không khí
+ Rất ít tan trong nước
+ Rất độc
- Gv: Viết bảng (theo sơ đồ tư duy tương tự của học sinh)
+ Gợi ý học sinh cách thu khí CO trong PTN (Có đẩy không khí được không? Thu bằng cách nào khác?)
+ Lưu ý tính độc: “Khí CO làm mất khả năng vận chuyển oxi của hemoglobin trong máu, ngộ độc nhẹ gây khó thở chóng mặt tức ngực nặng có thể hôn mê và tử vong.” Cho học sinh xem hình ảnh bài báo trên bản tin Chuyển động 24h ngày 17/11/2020: “4 người trong gia đình nhập viện do sử dụng than sưởi sau sinh, trong đó có 1 bệnh nhân 2 ngày tuổi, nhất là vào những ngày lạnh số ca nhập viện vì ngộ độc CO tăng lên, lưu ý tuyệt đối không đốt than sưởi trong phòng kín, khi gặp người bị ngộ đôc trước hết cần mở tất cả các cửa thông thoáng, cho nạn nhân nằm nghiêng bên phải, nhanh chóng đưa đến cơ sở y tế gần nhất.”
Hoạt động 2: Tìm hiểu tính chất hóa học và điều chế CO (8 phút)
Mục tiêu hoạt động
- Biết được CO là một oxit trung tính.
- Hiểu CO là chất khử, viết được PTPƯ chứng minh tính khử của CO
- Biết cách điều chế CO trong phòng thí nghiệm và trong công nghiệp.
Phương thức tổ chức hoạt động
* Oxit trung tính
- GV: “ Trong trò chơi khởi động các bạn đã nhắc lại 4 loại oxit , dựa vào kiến thức oxit đã được học ở cấp 2 các em hãy cho cô biết CO thuộc loại oxit gì?”
- HS: Oxit trung tính
- Gv: CO là oxit trung tính hay oxit không tạo muối, không tác dụng với nước, axit và dung dịch kiềm ở điều kiện thường
(giáo viên cbi giấy in sẵn nội dung → đính vào bảng)
* Tính khử
- GV: Trong các số oxi hóa của C mà các em đã biết, số oxi hóa của C trong CO bằng bao nhiêu, các em có dự đoán gì về tính chất oxi hóa khử của CO
- HS: Số oxh = +2 → trung gian, có cả tính oxi hóa và tính khử
- Gv: CO có cả tính oxi hóa và tính khử, trong đó tính khử là tính chất đặc trưng thể hiện khi tác dụng với các chất có tính oxi hóa như O2, oxit kim loại MxOy (Tính oxh sẽ tìm hiểu trong hóa học hữu cơ CO + CH3OH → CH3COOH). GV yêu cầu Hs lên bảng viết PTPƯ CO với O2 và MxOy
- Hs trình bày bảng : 2CO + O2 → 2CO2
yCO + MxOy → xM + yCO2
- Gv lưu ý: CO cháy cho ngọn lửa màu xanh lam, phản ứng tỏa nhiều nhiệt nên CO dùng làm nhiên liệu.
Một số oxit kim loại bị khử như Fe2O3, CuO → Tính chất này dùng trong luyện kim
* Điều chế:
- Gv: Các em hãy nghiên cứu sgk và cho biết cách điều chế CO trong PTN và trong CN
- Hs: PTN: HCOOH → CO + H2O (Gv viết bảng khi hs trả lời)
CN: C + H2O → CO + H2
→ Khí than ướt (44% CO)
CO2 + C → 2CO
→ Khí than khô (25% CO)
- Gv dán bảng phần nội dung này đã cbi sẵn, chiếu slide các hình ảnh điều chế CO trong PTN và CN
3. Tìm hiểu Cacbon đioxit (CO2)
* Tổ chức hoạt động trải nghiệm kết nối (5 phút)
- Gv: Cho hs quan sát đá khô, đây là CO2 ở trạng thái rắn, chúng ta sẽ tìm hiểu các TCVL và HH của CO2 thông qua “Thử thách khoa học”
- Gv chia lớp thành 4 nhóm, cung cấp dụng cụ hóa chất, yêu cầu học sinh đọc hướng dẫn, dự đoán hiện tượng, tiến hành thí nghiệm, nêu hiện tượng giải thích và rút ra kết luận về tính chất của CO2
- Các nhóm tiến hành thí nghiệm trong 2 phút, báo cáo kết quả

* Tìm hiểu tính vật lý CO2 (5 phút)
- Nhóm 1 báo cáo rút ra CO2 rắn dễ thăng hoa, khí CO2 ít tan trong nước
- Nhóm 2 báo cáo rút ra CO2 nặng hơn không khí, không duy trì sự cháy
- Gv kết luận và viết bảng :
+ CO2 là chất khí, không màu, nặng gấp 1,5 lần không khí
+ Ít tan trong nước
+ (dán bảng nội dung cbi sẵn)
Gv cung cấp thêm các ứng dụng của đá khô : tạo môi trường lạnh mà không ẩm để bảo quản thực phẩm, dùng trong tiệc cưới hoặc các hoạt động vui chơi khác.
* Tìm hiểu tính hóa học CO2 (7 phút)
- Nhóm 3, nhóm 4 báo cáo kết quả rút ra tính chất của CO2 là oxit axit có khả năng phản ứng với dd bazơ
- GV rút ra kết luận : CO2 là oxit axit
+ Tác dụng với nước
+ Tác dụng với dd bazơ
(HS lên bảng) CO2 + Ca(OH)2 → CaCO3 + H2O
CO2 dư + CaCO3 + H2O → Ca(HCO3)2
- Gv: CO2 không cháy và không duy trì sự cháy của nhiều chất, nên người ta thường dùng khí CO2 để dập tắt đám cháy. Vậy có đám cháy nào không dập tắt được được bằng CO2 không? Ngoài tính chất oxit axit, CO2 có tính chất oxi hóa khử nào khác, dựa vào số oxi hóa của CO2 các em hãy về tìm hiểu và trả lời cho cô trong buổi học sau.
* Tìm hiểu điều chế CO2 (3 phút)
- Gv : Dựa vào sgk hãy cho cô biết trong PTN, CO2 được điều chế bằng cách nào
- Hs trả lời Gv viết bảng : CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Gv hỏi học sinh cách thu khí CO2 (đẩy không khí, ngửa bình)
- Gv : Trong CN, có sản xuất CO2 không ?
Hs trả lời, Gv dán bảng nội dung đã cbi : Thu hồi từ quá trình đốt than, chuyển hóa khí thiên nhiên, nung vôi, lên men rượu…
4. Củng cố (7 phút)
- Gv kiểm tra việc hoàn thiện sơ đồ tư duy của học sinh, chọn 1 hs có kq tốt, dựa vào sơ đồ tư duy trên bảng gv đã hình thành trong tiết học, nhắc lại các kiên thức đã học của bài (3 phút)
- Gv cho học sinh trả lời câu hỏi củng cố bài học (trò chơi ai là triệu phú) (4 phút)
+ Câu 1: CO có tính chất:
A. Oxit axit, có tính khử mạnh.
B. Oxit bazơ, rất độc
C. Chất khí không màu, rất độc, oxit trung tính, có tính khử mạnh.
D. Chất khí, không màu, không mùi, có tính oxi hóa mạnh.
+ Câu 2: Để đề phòng bị nhiễm độc CO, người ta sử dụng mặt nạ với chất hấp phụ nào sau đây ?
A. Than mỡ
B. Than hoạt tính
C. Than nâu
D. Than bùn
+ Câu 3: Để loại CO2 lẫn trong khí CO, người ta dẫn hỗn hợp qua chất nào sau đây:
A. CuO
B. H2SO4 đặc
C. nước vôi trong
D. dd CuSO4
+ Câu 4: Điều nào sau đây là không đúng khi nói về “nước đá khô”
A. Có khả năng thăng hoa ở nhiệt độ thường.
B. Chất rắn, màu trắng.
C. Tạo môi trường lạnh và ẩm
D. Dùng để bảo quản thực phẩm.
- Gv cho học sinh làm một số bài tập tính toán nếu có thời gianB. Chất rắn, màu trắng.
C. Tạo môi trường lạnh và ẩm
D. Dùng để bảo quản thực phẩm.
1. Khử hoàn toàn 32gam Fe2O3 bằng khí CO dư, tính khối lượng kim loại thu được (Đ/s: 22,4g)
2. Dẫn 2,24l khí CO2 qua dung dịch nước vôi trong dư, tính khối lượng kết tủa thu được (Đ/s: 10g)
5. Hướng dẫn về nhà
- Học bài theo sơ đồ tư duy, làm đề trắc nghiệm củng cố
- Chuẩn bị phần C: Axit cacbonic và muối cacbonat (Tính chất và ứng dung?)
- Tìm hiểu hiệu ứng nhà kính và làm slide báo cáo (1 tuần)
- Đọc bài báo khoa học “Biến đổi khí hậu vẫn đang tiếp diễn” và trả lời các câu hỏi kèm theo
Tin liên quan
- Công bố đề minh họa cho cấu trúc định dạng đề thi tốt nghiệp THPT từ 2025
- Bí quyết đạt điểm 9, 10 môn Sinh tốt nghiệp THPT
- [Bí quyết đạt điểm 9, 10 bài thi Tốt nghiệp THPT năm 2021] MÔN TOÁN
- [Bí quyết đạt điểm 9, 10 bài thi Tốt nghiệp THPT năm 2021] MÔN GDCD
- [Bí quyết đạt điểm 9, 10 bài thi Tốt nghiệp THPT năm 2021] MÔN ĐỊA LÍ







